应用案例:“眼见为实”HS-AFM实时成像粘连蛋白介导DNA环挤出的过程
应用案例(超高速视频级原子力显微镜-HS-AFM):“眼见为实”HS-AFM实时成像粘连蛋白介导DNA环挤出的过程
翻译整理:北京佰司特科技有限责任公司
超高速视频级原子力显微镜(High-Speed Atomic Force Microscope,HS-AFM)由日本 Kanazawa 大学 Prof. Ando 教授团队研发,日本RIBM公司(生体分子计测研究所株式会社,Research Institute of Biomolecule Metrology Co., Ltd)商业化的产品,可以达到视频级成像的商业化原子力显微镜。HS-AFM突破了传统原子力显微镜“扫描成像速慢”的限制,能够在液体环境下超快速动态成像,分辨率为纳米水平。样品无需特殊固定,不影响生物分子的活性,尤其适用于生物大分子互作动态观测。超高速视频级原子力显微镜HS-AFM主要有两种型号,SS-NEX样品扫描(Sample-Scanning HS-AFM)以及PS-NEX探针扫描(Probe-Scanning HS-AFM)。推出至今,全球已有100多位用户,发表 SCI 文章 300 余篇,包括Science, Nature, Cell 等顶级杂志。
相较于目前市场上的原子力显微镜成像设备,HS-AFM突破了 “扫描成像速慢”的限制,扫描速度高可达 20 frame/s,并且有 4 种扫描台可供选择。样品无需特殊固定染色,不影响生物分子的活性,尤其适用于生物大分子互作动态观测。液体环境下直接检测,超快速动态成像,分辨率为纳米水平。探针小,适用于生物样品;悬臂探针共振频率高,弹簧系数小,避免了对生物样品等的损伤。悬臂探针可自动漂移校准,适用于长时间观测。采用动态PID控制,高速扫描时仍可获得清晰的图像。XY轴分辨率2nm;Z轴分辨率0.5nm。
HS-AFM不仅拥有超高扫描速率与原子级别分辨率,而且具有操作的简易性,使得对单分子动态过程的捕捉变得十分方便,为科研工作者研所和理解生物物理、生物化学、分子生物学、病毒学以及生物医学等领域的单分子动态过程提供了一款强大的工具。
全新的HS-AFM采用了新的高频微悬臂架构,更低噪音、更高稳定性的2控制器,高速扫描器,缓冲防震设计,主动阻尼,动态PID,驱动算法优化,多种前沿技术,可以实现在超高速下获取高分辨的生物样品信息。新系统整合了基于工作流程的操作软件,直观的用户界面与流程化、自动化的设置使得研究人员可以专注于实验设计,不需要复杂的操作和条件设置,快速获取数据,加速研究的产出。

Cohesin mediates DNA loop extrusion by a “swing and clamp” mechanism
CELL. VOLUME 184, ISSUE 21, P5448-5464.E22, OCTOBER 14, 2021
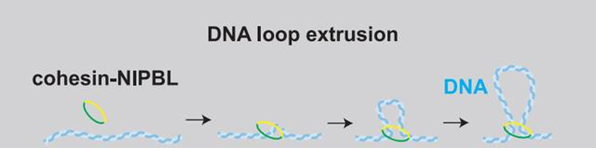
基因组DNA折叠形成环状以及拓扑关联结构域(Topologically associating domains,TADs),从而组成了基因组复杂的三维结构,这些三维结构具有重要的结构和调控作用。先前的研究已经逐渐揭示出基因组结构是由染色体结构维持SMC(Structural maintenance of chromosomes)蛋白复合物所介导的环挤出(DNA loop extrusion)过程形成的(图1)。单分子层面的研究表明SMC蛋白复合体和Cohesin蛋白的确能够将DNA挤压形成环状。因此,关于基因组的三维结构形成研究者们提出了“环挤出假说”,认为染色体结构维持的SMC复合物组织就基因组的拓扑结构,并通过环挤出来实现这一功能。但是这一过程的具体细节是如何进行的还不得而知。
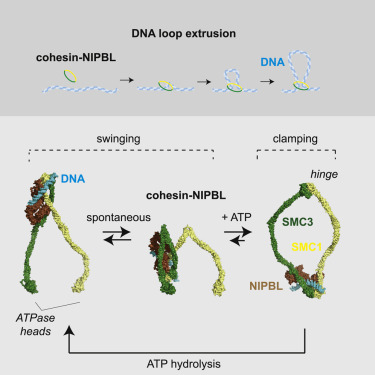
奥地利维也纳生物中心 (VBC)分子病理学研究所Jan-Michael Peters研究组发现粘连蛋白通过“摆动和钳夹”机制介导 DNA 环挤出。2021年10月7日出版的《细胞》杂志发表了这一成果。
他们分析了人类粘连蛋白-NIPBL 复合物如何介导环挤出,并使间期细胞中的染色质折叠。 他们已经确定了环挤出所需的 DNA 结合位点和大规模构象变化,并确定了这些是如何协调的。他们的结果表明 DNA 通过自发的 50 nm 摆动的粘连蛋白铰链转移,将 DNA 交给 SMC3 的 ATPase 头部,在那里结合 ATP,然后DNA 被 NIPBL 夹住。
在这个过程中,NIPBL 从铰链“跳跃”到 SMC3 头部,从而可能将自发铰链摆动与 ATP 依赖性 DNA 夹紧结合起来。 这些结果揭示了粘连蛋白-NIPBL 和可能的其他染色体结构维持 (SMC)复合物如何介导环挤出的机械原理。
该实验过程通过借助日本RIBM公司研发的超高速视频原子力显微镜HS-AFM来完成,HS-AFM突破了传统原子力显微镜“扫描成像速慢”的限制,能够实现在液体环境下超快速动态成像,分辨率为纳米水平。待测样品无需特殊固定,不影响生物分子的活性,尤其适用于生物大分子互作动态观测。
目前,一些体外的生化重构实验一定程度上已经证实了环挤出假说,这些结果证明SMC蛋白与Cohesin蛋白会以2.1kb/s的速度挤压DNA,并且这一过程依赖于ATP酶活性(图2)。但限于实验分辨率等问题,环挤出的过程是如何实现的具体细节还不得而知。
DNA环挤出过程中具体的构象变化是如何发生的呢?为了揭开这一过程的全貌,作者们应用了高速原子力显微镜(High-speed atomic force microscopy,HS-AFM)对Cohesin进行了实时成像。
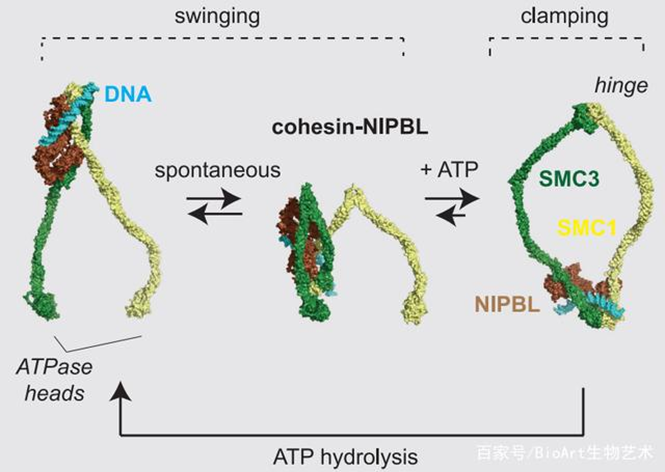
DNA环挤出“摆-夹”“Swing and clamp”模型
在ATP存在的情况下的,Cohesin三聚体复合物中会在环状、杆状以及弯曲状构象之间的变化。作者们发现DNA是通过Cohesin蛋白铰链的弯曲进而易位的,这样将DNA转移到SMC3的ATP酶活性头部,在该位置与ATP结合,DNA被NIPBL夹住。在此过程中NIPBL从铰链向SMC3头部移动,引发铰链区域的自发摆动以及ATP依赖的DNA结合,从而形成一个循环,使得DNA从铰链延伸到SMC3的头部,在此循环周期的末尾,DNA片段可以转移到SMC1的头部。由此,作者们提出了DNA环挤出的“摆-夹”“Swing and clamp”模型,这类似于抓娃娃机的小爪子,可以将通过铰链的弯曲伸出机械手“抓住”DNA,然后上提,从而通过一次次循环促使DNA逐步环挤出。
Cohesin mediates DNA loop extrusion by a “swing and clamp” mechanism
Abstract: Structural maintenance of chromosomes (SMC) complexes organize genome topology in all kingdoms of life and have been proposed to perform this function by DNA loop extrusion. How this process works is unknown. Here, we have analyzed how loop extrusion is mediated by human cohesin-NIPBL complexes, which enable chromatin folding in interphase cells. We have identified DNA binding sites and large-scale conformational changes that are required for loop extrusion and have determined how these are coordinated. Our results suggest that DNA is translocated by a spontaneous 50 nm-swing of cohesin’s hinge, which hands DNA over to the ATPase head of SMC3, where upon binding of ATP, DNA is clamped by NIPBL. During this process, NIPBL “jumps ship” from the hinge toward the SMC3 head and might thereby couple the spontaneous hinge swing to ATP-dependent DNA clamping. These results reveal mechanistic principles of how cohesin-NIPBL and possibly other SMC complexes mediate loop extrusion.
作者通过超高速视频级原子力显微镜实时成像,实现了对Cohesin促使的DNA环挤出过程的全纪录,从而能够将DNA从一个结合位点带到另一个结合位点,揭开了SMC复合体进行基因组的折叠的以及促进复杂基因组三维拓扑结构形成的机制。
原文链接:
https://doi.org/10.1016/j.cell.2021.09.016
这项工作的完成主要借助了日本RIBM公司研发的超高速视频原子力显微镜HS-AFM,HS-AFM突破了传统原子力显微镜“扫描成像速慢”的限制,能够实现在液体环境下超快速动态成像,分辨率为纳米水平。待测样品无需特殊固定,不影响生物分子的活性,尤其适用于生物大分子互作动态观测。推出至今,全球已有100多位用户,发表SCI论文300余篇,其中包括Science, Nature, Cell 等顶级杂志。
小结:使用HS-AFM获得的高空间&时间分辨率的视频图像,可以准确地反应生物大分子的运动状态,用于定量研究。
新品推荐——日本RIBM公司研发的超高速视频原子力显微镜HS-AFM来到中国
为了更好地服务国内客户,北京佰司特科技有限责任公司将这款超高速视频级原子力显微镜引进中国,如果您有科研上的需要,欢迎致电联系我们!
地址: 北京市北京市朝阳区劲松三区甲302楼华腾大厦7层703B室
电话: 010-67751532 邮箱: best_science@163.com
北京佰司特科技有限责任公司 (https://www.best-sciences.com)
类器官串联芯片培养仪-HUMIMIC;灌流式细胞组织类器官代谢分析仪-IMOLA;光片显微镜-LSM-200;
蛋白稳定性分析仪-PSA-16;单分子质量光度计-TwoMP;超高速视频级原子力显微镜-HS-AFM;
全自动半导体式细胞计数仪-SOL COUNT;农药残留定量检测仪—BST-100;台式原子力显微镜-ACST-AFM;微纳加工点印仪-NLP2000/DPN5000;
- 2024-05-01
- 2024-05-01
- 2024-05-01
- 2024-04-03
- 2024-04-03
- 2024-03-28
- 2024-03-16
- 2023-10-13
- 2023-10-01
- 2023-09-15
- 2023-09-15
- 2023-09-06
- 2023-09-01
- 2023-08-14
- 2023-08-14
